【适应症】
本品是一种 Trop-2 靶向抗体和拓扑异构酶抑制剂偶联物,用于治疗既往接受过内分泌治疗和化疗的患有不可切除或转移性、激素受体 (HR) 阳性、人类表皮生长因子受体 2 (HER2) 阴性 (IHC 0、IHC 1+ 或 IHC 2+/ISH-) 乳腺癌的成年患者。
【推荐剂量】
本品的推荐剂量为 6 mg/kg,静脉输注,每 3 周(21 天为一个周期)一次,持续用药直至病情进展或出现不可接受的毒性。
【不良反应】
最常见的不良反应(≥20%)包括实验室异常,包括口腔炎、恶心、疲劳、白细胞减少、钙减少、脱发、淋巴细胞减少、血红蛋白减少、便秘、中性粒细胞减少、干眼症、呕吐、ALT 升高、角膜炎、AST 升高和碱性磷酸酶升高。
【药理作用】
本品是一种靶向 Trop-2 的抗体-药物偶联物。该抗体是一种人源化的抗 Trop2 IgG1。小分子 DXd 是一种拓扑异构酶 I 抑制剂,通过可裂解的接头与抗体连接。在与细胞(包括肿瘤细胞)上的 Trop2 结合后,本品会被溶酶体酶内化和细胞内接头裂解。释放后,可透过膜的 DXd 会导致 DNA 损伤和细胞凋亡。本品在乳腺癌小鼠模型中具有抗肿瘤活性。
【使用方法】
-本品仅供静脉输注。请勿静脉推注或快速滴注。请勿使用氯化钠注射液。
-使用治疗前用药以预防输液反应和恶心呕吐。
-治疗前用药、伴随用药和所需的眼部护理:
在有心肺复苏药物和设备的环境中使用本品。在开始使用本品时、治疗期间每年一次、治疗结束时以及根据临床指征进行眼科检查,包括视力测试、裂隙灯检查(荧光素染色)、眼压和眼底镜检查。
本品的治疗前用药和伴随用药见表 1。
在前 2 个本品输注周期中,监测患者输液体相关反应至少 1 小时。如果没有观察到输液相关反应,则在随后的所有输注周期中监测患者至少 30 分钟。
表 1:给药前用药和伴随用药

【剂量调整】
不良反应的剂量调整
表 2 列出了不良反应的推荐剂量减少水平。
表 2:DATROWAY 不良反应的推荐剂量减少

剂量减少后,不要重新增加本品剂量。对于无法耐受每 3 周一次静脉注射 3 mg/kg 的患者,应永久停用本品。
表 3 列出了针对本品不良反应的推荐剂量调整。
表 3:针对不良反应的 DATROWAY 剂量调整
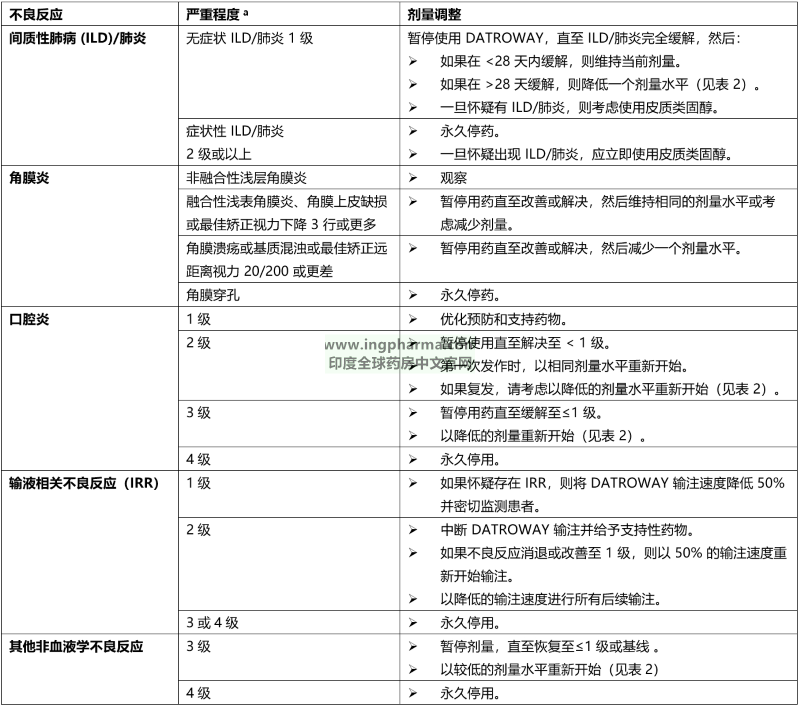
a 毒性等级符合美国国家癌症研究所不良事件常用术语标准 (NCI CTCAE) 5.0 版。
【延迟或遗漏给药】
如果计划剂量延迟或错过,请尽快给药;不要等到下一个计划周期。调整给药时间表以保持剂量间隔 3 周。
【过量处理】
无相关信息
【注意事项】
-间质性肺病 (ILD) 和肺炎:
本品可导致严重和致命的 ILD/肺炎病例。监测 ILD/肺炎的新发的或恶化的症状和体征。如果怀疑患有 ILD/肺炎,请暂停使用本品并开始使用皮质类固醇。对于确诊为 2 级或更高级别 ILD/肺炎的患者,请永久停用本品。
-眼部不良反应:
本品可引起眼部不良反应,包括干眼症、角膜炎、睑缘炎和睑板腺功能障碍、流泪增多、结膜炎和视力模糊。使用本品治疗期间,应监测患者是否出现眼部不良反应。建议患者使用不含防腐剂的润滑眼药水,并在使用本品治疗期间避免佩戴隐形眼镜。根据眼部不良反应的严重程度,延迟剂量、减少剂量或永久停用本品。如果出现任何新的或恶化的眼部症状和体征,请将患者转诊给眼科专业人员。
-口腔炎/口腔黏膜炎:
本品可引起口腔炎,包括口腔溃疡和口腔黏膜炎。建议患者在开始治疗时使用含类固醇的漱口水,并在输注本品期间将冰块或冰水含在口中。根据不良反应的严重程度,暂停、减少剂量或永久停用本品。
-胚胎-胎儿毒性:
本品可导致胎儿伤害。告知患者本品对胎儿的潜在风险并使用有效的避孕措施。
【禁忌】
无
【特殊人群】
-妊娠期:
根据其作用机制,本品给孕妇服用时可能会造成胎儿伤害。
-哺乳期:
建议女性在使用本品治疗期间以及最终剂量后至少1个月内不要母乳喂养。
-儿童:
尚未确定本品对儿童患者的安全性和有效性。
-老年患者:
≥65 岁患者发生 3 级及严重不良反应的几率 (分别为 42% 和 25%) 高于 <65 岁患者 (分别为 33% 和 15%)。在 TROPION-Breast01 研究中,≥65 岁患者与年轻患者之间在安全性或有效性方面未观察到其他有意义的差异。
-肾损伤患者:
对于轻度或中度肾功能损害的患者,不建议进行剂量调整[Cockcroft-Gault估计肌酐清除率(CLcr)为30至89 mL/min]。
对于严重肾功能损害(CLcr<30 mL/min)的患者,尚未确定本品的推荐剂量
轻度和中度肾功能不全[肌酐清除率 (CLcr)30 至 <90 mL/min]患者中观察到 ILD/肺炎发生率较高。监测肾功能不全患者是否出现不良反应增加,包括呼吸道反应。对于轻度至中度肾功能不全患者,不建议调整剂量。严重肾功能不全(CLcr <30 mL/min)对本品或 DXd 药代动力学的影响尚不清楚。
-肝损伤患者:
对于轻度肝功能不全(总胆红素≤ULN 和任何 AST>ULN 或总胆红素>1 至 1.5 倍 ULN 和任何 AST)患者,建议无需调整剂量。
对于中度肝功能不全(总胆红素>1.5 至 3 倍 ULN 和任何 AST)患者,数据有限。监测中度肝功能不全患者是否出现不良反应增加。
对于重度肝功能不全(总胆红素>3 倍 ULN 和任何 AST)患者,尚未确定本品的推荐剂量。
【药物相互作用】
无相关信息
【贮藏】
将药瓶放在原包装盒中,在 2ºC 至 8ºC的冰箱中避光保存。
请勿冷冻。请勿摇晃配制或稀释后的溶液。
- 产品名称:DATROWAY
- 通用名称:datopotamab deruxtecan-dlnk
- 剂型:冻干粉
- 规格:100mg/瓶
- 生产厂家:Daiichi Sankyo 日本第一三共制药
请按药品说明书或在药师指导下购买和使用

 下载app
下载app