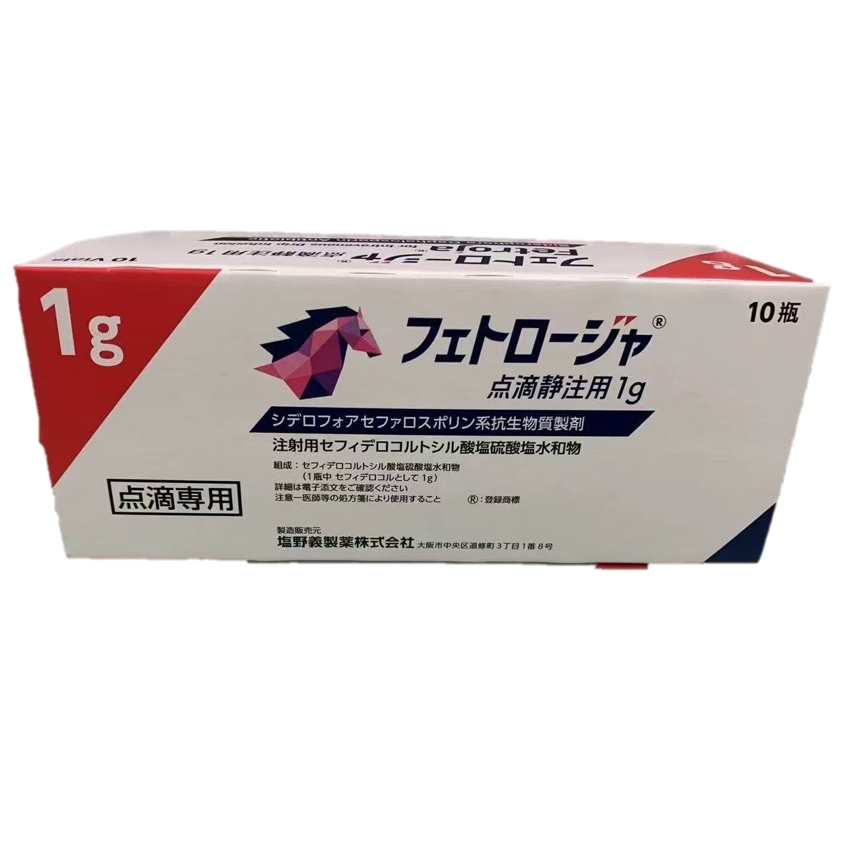
【适应症】
本品是一种头孢菌素类抗菌剂,适用于治疗18岁及以上患者的由易感革兰氏阴性菌微生物:大肠埃希菌、肺炎克雷伯菌、奇异变形杆菌、铜绿假单胞菌和阴沟肠杆菌复合体导致的以下感染:
-复杂性尿路感染(cUTI),包括肾盂肾炎。
-医院获得性细菌性肺炎和呼吸机相关细菌性肺炎(HABP/VABP)。
为了减少耐药细菌的产生并维持本品和其他抗菌药物的有效性,本品应仅用于治疗或预防已被证实或强烈怀疑由革兰氏阴性细菌引起的感染。
【推荐剂量】
-CLcr 60-119mL/分患者:
推荐剂量为2g,静脉输注,持续输注3小时,每8小时给药一次。推荐的治疗时间为7-14天,实际治疗时间根据患者的临床反应而定。
-对于CLcr<60mL/分患者,包括接受间歇性血液透析(HD)或连续性肾脏替代治疗(CRRT) 的患者,以及CLcr≥120 mL/分的患者:
应进行剂量调整,详见《剂量调整》
【剂量调整】
-CLcr<60mL/分患者,包括接受间歇性血液透析(HD)患者的剂量调整:
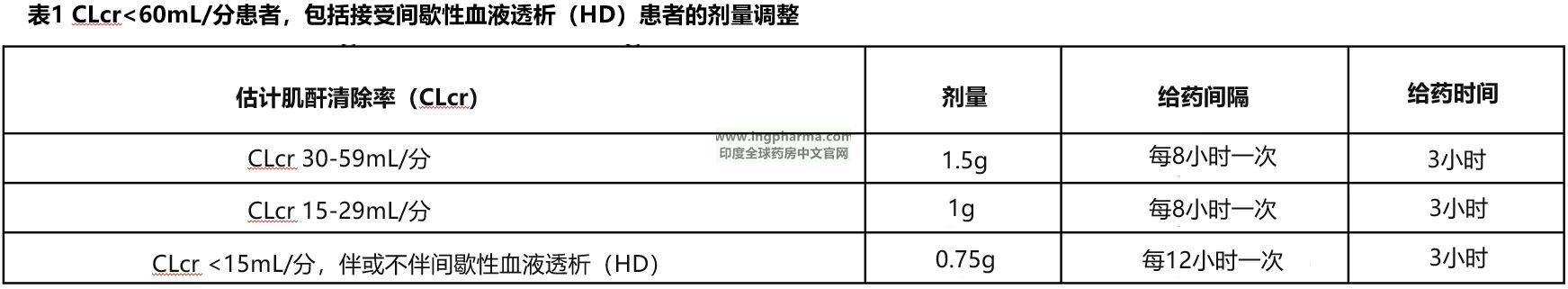
-接受连续性肾脏替代治疗(CRRT) 患者的剂量调整:
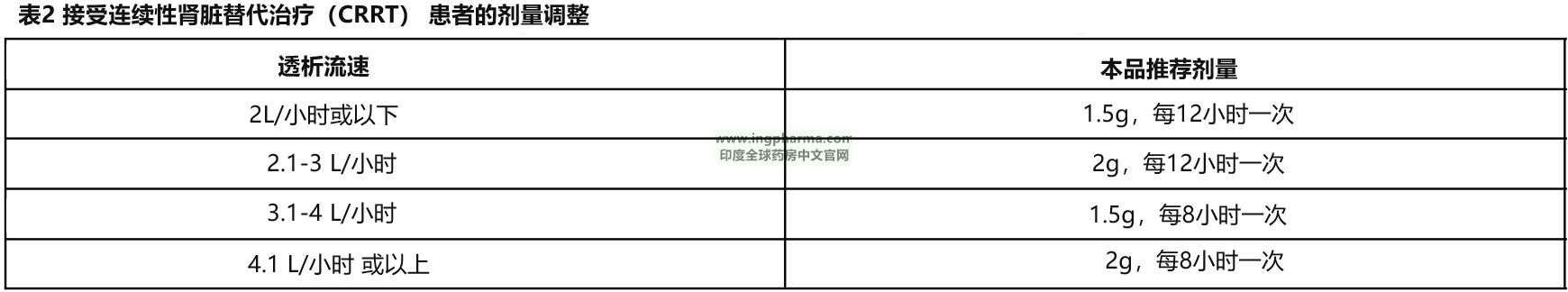
-CLcr≥120 mL/分患者的剂量调整:
每次2g,每6小时一次,静脉输注,每次持续输注3小时。
【不良反应】
-复杂性尿路感染(cUTI):
最常见不良反应(≥2%):腹泻,输液部位反应、便秘、皮疹、念珠菌病、咳嗽、升高肝功能检查、头痛、低钾血症、恶心和呕吐。
-医院获得性细菌性肺炎和呼吸机相关细菌性肺炎(HABP/VABP):
最常见的不良反应(≥4%):肝功能升高、低钾血症、腹泻、低镁血症和心房颤动
【使用方法】
-本品静脉输注,每次持续输注3小时。
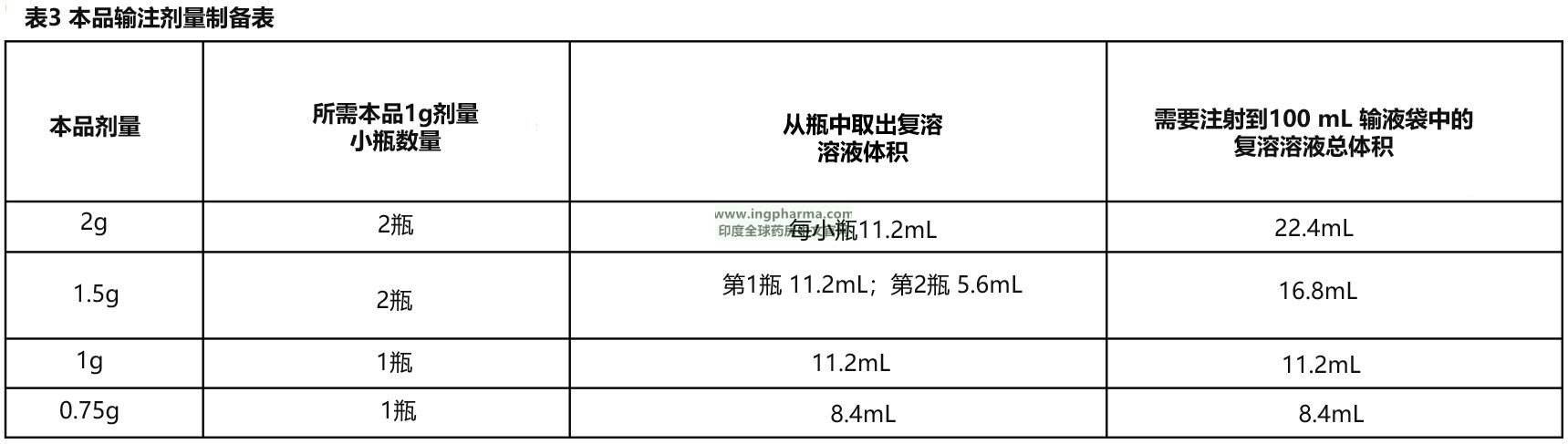
-本品复溶需使用10 mL 0.9% 氯化钠注射液或 5% 葡萄糖注射液,轻轻摇晃以使其溶解。
-让药瓶静置,直至药液表面产生的泡沫消失(通常在2分钟内)。复溶溶液最终体积约为11.2mL,浓度为0.089g/mL。
-然后,将复溶后的溶液取出注入至100ml含有0.9%氯化钠注射液或5% 葡萄糖注射液的输液袋中。
-本品注射前,应目视检查溶液是否有颗粒物和变色。通常本品复溶后溶液应为透明、无色。
【服用过量处理】
没有关于与本品过量相关的临床体征和症状的信息。患者接受大于推荐剂量方案的剂量并可能出现意外的不良反应,应仔细监测患者并给予相关支持性治疗,应考虑停药或中断治疗。大约 60% 的本品可通过 3 至 4 小时的血液透析清除。
【注意事项】
-革兰氏阴性细菌感染且碳青霉烯类耐药患者全因死亡率增加:
与接受最佳治疗疗法(BAT)的患者相比,在本品治疗患者中观察到全因死亡率增加 。在 cUTI 和 HABP/VABP 患者中,密切监测患者对治疗的临床反应。
-超敏反应:
在接受β内酰胺类抗菌药物治疗的患者中,已报道严重和偶尔致命的超敏反应(过敏性)。在本品治疗中观察到超敏反应。交叉超敏反应可能发生在有青霉素过敏病史的患者中 。如果发生过敏反应,请停用本品。
-艰难梭菌相关性腹泻 (CDAD):
接受全身性抗菌药物治疗患者中,包括本品,已报道艰难梭菌相关性腹泻病例。本品治疗期间,需要评估患者是否发生腹泻。
-癫痫发作和其他中枢神经系统 (CNS) 不良反应:
本品治疗期间,已报道中枢神经系统不良反应(如癫痫发作)。如果发生局灶性震颤、肌阵挛或癫痫发作,请评估患者以确定是否应停用本品。
【禁忌】
本品禁用于已知有严重对本品、本品其他成份和其他β-内酰胺类抗菌药物过敏者。
【特殊人群】
-孕妇:
无相关临床数据确认本品相关药物风险。
-哺乳期:
无相关临床数据。
-儿童:
本品用于18岁以下儿童患者的安全性和有效性尚未确立。
-老年人:
本品用于老年人患者的临床反应与年轻人无差异。
-肾损伤患者:
本品剂量调整,详见《剂量调整》
-肝损伤:
本品用于肝功损伤患者的药代动力学尚未得到评估。肝功损伤预计不会改变本品代谢,因为肝脏不是本品主要代谢通道。肝功损伤患者,本品无需剂量调整。
【药物相互作用】
使用其他检测方法确认试纸检测的阳性结果(尿蛋白、酮体或潜血)。
【药理作用】
本品(S-649266)是一种新型注射用铁载体头孢菌素抗生素,与其他β-内酰胺类抗生素一样,具有抑制细胞壁合成的作用机制。本品对青霉素结合蛋白(PBP)3 表现出高亲和性,在与青霉素的竞争结合试验中,青霉素结合蛋白(PBP)3 与铜绿假单胞菌、大肠杆菌、肺炎克雷伯菌及鲍曼不动杆菌的细胞壁分区形成有关。当使本品作用于这些菌株时,观察到细胞的伸长,这被认为是由于本品对 PBP 3 的抑制作用。本品与其他β-内酰胺类抗生素在两个主要方面不同。第一,本品 对 IMP-1(金属β内酰胺酶之一)、VIM-2(Veronaintegron metallo-β-lactamase,B 类碳青霉烯酶之一))、L1、KPC-3(K. pneumoniae carbapenemase-3,A 类碳青霉烯酶之一)、OXA-23、OXA-24/40、OXA-48(OXA 指 oxacillinase ,D 类碳青霉烯酶之一)及 NDM-1(New Delhi metallo β lactamase ,B 类碳青霉烯酶之一)等含碳青霉烯酶的 A~D 类β-酰胺酶稳定。此外,本品显 示 出 对 阴 沟 肠 杆 菌 的 染 色 体 AmpC ( Class Campicillinase,C 类β-内酰胺酶之一)的高稳定性,并且在铜绿假单胞菌和阴沟肠杆菌中诱导染色体 AmpC 的能力低。由于这种针对β- 内酰胺酶的稳定性特征,本品对各种类别的各种产生β-内酰胺酶的细菌均表现出强大的抗菌活性。第二,由于本品在3 位侧链上有一个邻苯二酚基团,因此它与铁离子形成络合物,并且由于其独特的利用细菌吸收铁的机制入侵到细菌体内,因此可以避开细菌特有的渗透障碍,例如多药外排泵的过量表达(这是对多种抗生素的主要耐药因素)以及外膜孔蛋白缺损等(外膜孔蛋白是β- 内酰胺类抗生素的主要渗透途径)。由于这些特性,本品被认为对几乎所有的革兰氏阴性菌都具有强大的抗菌活性。
【贮藏】
-未开封:
2~8℃温度冷藏保存;避光保存。
-复溶后溶液:
在室温下最长保存1小时;如果超过1小时,请丢弃。
-稀释后输液药液:
在输液袋中本品稀释后药液在室温下保存最长6小时;在2°C-8°C温度下冷藏且避光保存最长24小时;然后,室温下6小时内完成输注给药。
- 产品名称:FETROJA,Fetcroja
- 通用名称:Cefiderocol
- 剂型:冻干粉
- 规格:1g*10支
- 生产厂家:SHIONOGI INC. 盐野义制药
请按药品说明书或在药师指导下购买和使用

 下载app
下载app